Crean una píldora viviente para combatir infecciones resistentes a los antibióticos
January 26, 2023 Bienestar , NoticiasUnos científicos han diseñado la primera “píldora viva” para tratar infecciones pulmonares. El tratamiento va dirigido contra la Pseudomonas aeruginosa, una bacteria que es resistente de manera natural a muchos tipos de antibióticos y que es una fuente común de infecciones en los hospitales.
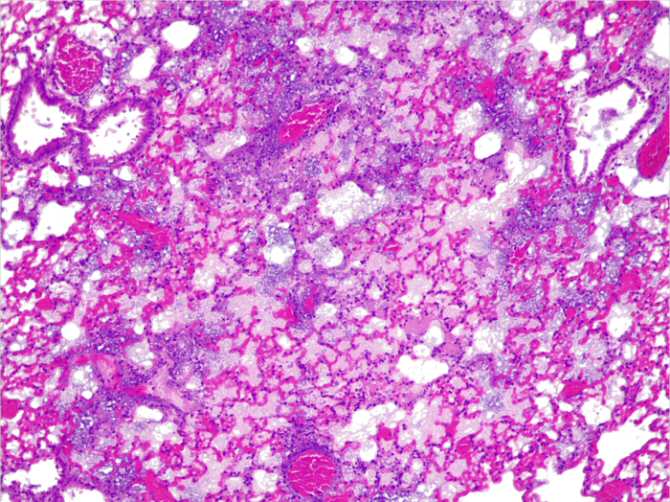
Esta imagen muestra una sección transversal de un pulmón de ratón infectado con Pseudonomas aeruginosa. El ratón fue tratado con una versión de Mycoplasma pneumoniae que no produce moléculas terapéuticas, lo que provocó una neumonía grave. Ello se caracteriza por la infiltración masiva de células inflamatorias en los septos alveolares, lo que resulta en la pérdida de aire en los alvéolos. / Rocco Mazzolini / CRG. CC BY-SA
El tratamiento consiste en utilizar una versión modificada de la bacteria Mycoplasma pneumoniae, eliminando su capacidad patógena y adaptarla para que, en su lugar, ataque a la P. aeruginosa. La bacteria modificada se usa en combinación con dosis bajas de antibióticos que no serían eficaces por sí solas.
El trabajo lo ha llevado a cabo un equipo que incluye a investigadores del Centro de Regulación Genómica (CRG) en Barcelona y la Universidad Internacional de Cataluña.
El equipo observó que el uso del tratamiento en ratones redujo significativamente las infecciones pulmonares. La “píldora viva” duplicó la tasa de supervivencia del ratón en comparación con la opción de no usar ningún tratamiento. La administración de una única dosis alta del tratamiento no mostró signos de toxicidad en los pulmones. Una vez que el tratamiento hubo terminado su curso, el sistema inmune innato eliminó las bacterias modificadas en un período de cuatro días.
En el estudio también han participado la empresa Pulmobiotics (impulsada por el CRG), el Instituto de Investigaciones Biomédicas August Pi i Sunyer (IDIBAPS) en Barcelona, el Hospital Clínic de Barcelona y el Instituto de Agrobiotecnología (IdAB), un instituto de investigación del CSIC y del gobierno de Navarra, en España.
Las infecciones causadas por P. aeruginosa son difíciles de tratar porque la bacteria vive en comunidades que forman biopelículas. Las biopelículas pueden adherirse a varias superficies del cuerpo, formando estructuras impenetrables a modo de búnker que escapan al alcance de los antibióticos.
Las biopelículas de P. aeruginosa crecen en la superficie de los tubos endotraqueales utilizados por pacientes en estado crítico quienes, por lo tanto, requieren ventiladores mecánicos para respirar. Esto causa neumonía asociada al ventilador (NAV), una afección que afecta hasta uno de cada cuatro (9-27%) pacientes que requieren intubación. La incidencia supera el 50% en el caso de los pacientes intubados por COVID-19 grave. La NAV puede prolongar la estancia en la unidad de cuidados intensivos hasta un periodo de trece días, y tiene una tasa de mortalidad que alcanza a uno de cada ocho pacientes (9-13%).
La píldora viviente basada en la M. pneumoniae fue diseñada para disolver biopelículas. El equipo científico modificó la bacteria para proporcionarle la capacidad de producir varias sustancias, incluidas las piocinas, toxinas producidas de forma natural por las bacterias para matar o inhibir el crecimiento de varias cepas de Pseudomonas. Para probar su eficacia, recogieron biopelículas de P. aeruginosa de los tubos endotraqueales de pacientes en unidades de cuidados intensivos. Comprobaron que el tratamiento atraviesa la barrera y disuelve con éxito las biopelículas.
«Hemos desarrollado un ariete que asedia a las bacterias resistentes a los antibióticos. El tratamiento abre orificios en las paredes celulares y crea unos puntos de entrada fundamentales para que los antibióticos las invadan y eliminen la infección en su origen. Creemos que es una nueva estrategia prometedora para abordar la principal causa de mortalidad hospitalaria», explica la Dra. María Lluch, directora científica de Pulmobiotics, coautora del estudio e investigadora de la Universidad Internacional de Cataluña.
Con el objetivo de utilizar la “píldora viva” para tratar la NAV, se llevarán a cabo más pruebas antes de llegar a la fase de ensayo clínico. Se prevé administrar el tratamiento con un nebulizador, un dispositivo que transforma el medicamento líquido en una niebla que se inhala a través de una boquilla o de una máscara.
M. pneumoniae es una de las especies de bacterias más pequeñas conocidas. El Dr. Luis Serrano, director del CRG, tuvo la idea de modificar la bacteria y usarla como una “píldora viva” hace dos décadas. El Dr. Serrano es especialista en biología sintética, un campo que implica la ingeniería de organismos para que tengan habilidades nuevas y útiles. Con solo 684 genes y sin pared celular, la relativa simplicidad de M. pneumoniae la hace ideal para la ingeniería biológica orientada a aplicaciones específicas.
Una de las ventajas de usar M. pneumoniae para tratar enfermedades respiratorias es que está adaptada de manera natural al tejido pulmonar. Después de administrar la bacteria modificada, viaja directamente al origen de una infección respiratoria, donde se establece como una fábrica temporal y produce una serie de sustancias terapéuticas.
Al demostrar que M. pneumoniae puede usarse contra las infecciones en el pulmón, el estudio abre la puerta al desarrollo de nuevas cepas de la bacteria orientadas a combatir otros tipos de enfermedades respiratorias como el cáncer de pulmón o el asma. «La bacteria se puede modificar con diversas cargas activas distintas, ya sean citoquinas, nanoanticuerpos o defensinas. El objetivo es diversificar el arsenal de la bacteria modificada y liberar su potencial en el tratamiento de una gama de enfermedades complejas», explica el Profesor de Investigación ICREA Dr. Luis Serrano.
Además de diseñar la “píldora viva”, el laboratorio del Dr. Serrano también está utilizando su experiencia en biología sintética para diseñar nuevas proteínas que pueden ser administradas por la M. pneumoniae. El equipo está utilizando estas proteínas para tratar la inflamación causada por las infecciones de P. aeruginosa.
Aunque la inflamación es una respuesta natural del cuerpo en reacción a una infección, la inflamación excesiva o prolongada puede dañar al tejido pulmonar. La respuesta inflamatoria es orquestada por el sistema inmune, que libera proteínas mediadoras como las citoquinas. Un tipo de citoquina, IL-10, tiene propiedades antiinflamatorias bien conocidas, lo que, por tanto, hace que sea de creciente interés terapéutico.
El estudio se titula “Engineered live bacteria suppress Pseudomonas aeruginosa infection in mouse lung and dissolve endotracheal-tube biofilms”. Y se ha publicado en la revista académica Nature Biotechnology.
En otra investigación, publicada en la revista académica Molecular Systems Biology, el grupo de investigación del Dr. Serrano utilizó ModelX y FoldX, dos programas informáticos para el diseño de proteínas, para crear nuevas versiones de IL-10 optimizadas para el tratamiento de la inflamación. Estas nuevas citoquinas tienen nuevas propiedades que mejoran su eficiencia y afinidad.
El equipo científico diseñó cepas de M. pneumoniae que expresan estas nuevas citoquinas y probó su eficacia en los pulmones de ratones con infecciones agudas por P. aeruginosa. Los investigadores mostraron que las versiones diseñadas de IL-10 eran significativamente más efectivas para reducir la inflamación en comparación con la citoquina IL-10 natural.
Ariadna Montero Blay, coautora de aquel estudio en Molecular Systems Biology, indica que «las soluciones bioterapéuticas como M. pneumoniae proporcionan vehículos ideales para superar las limitaciones tradicionales de las citoquinas y desbloquear su enorme potencial en el tratamiento de diversas enfermedades humanas. La ingeniería de citoquinas como moléculas terapéuticas fue fundamental para combatir la inflamación. Otras enfermedades pulmonares como el asma o la fibrosis pulmonar también podrían beneficiarse de este enfoque».



