Cristales de laboratorio para regenerar dientes y huesos
June 1, 2018 Bienestar , NoticiasUna nueva técnica permite cultivar tejidos minerales como el esmalte dental a partir de proteínas.
Las técnicas existentes no son capaces de regenerar el esmalte dental. / RGERBER / PIXABAY
Los tejidos duros del cuerpo no suelen tener células. El más duro, el esmalte dental, es casi completamente inorgánico: el 97% de su composición es mineral de hidroxiapatita. Así permite a los dientes resistir los elementos duros, ácidos o calientes que entran en la boca. Pero eso también significa que, una vez se desgasta el esmalte, no hay forma de recuperarlo. Un equipo internacional de bioingenieros ha desarrollado una técnica “sumamente fácil” para sintetizar materiales orgánicos y cristalinos con la estructura del esmalte, descrita hoy en la revista Nature Communications. Los investigadores ya están probando el nuevo método en medicina regenerativa de dientes y huesos.
“Cuando un paciente viene a la clínica quejándose de dolor, por ejemplo al tomar bebidas frías, tiene hipersensibilidad dental”, explica el dentista e investigador postdoctoral de Queen Mary University (Londres) Sherif Elsharkawy, primer autor del estudio. El desgaste del esmalte deja al descubierto pequeñas terminaciones nerviosas del diente que hacen de cualquier refresco un sufrimiento. “Solemos aplicar una especie de barniz que cubre el diente para paliar el dolor, pero no es muy resistente ni duradero”, añade. Según los investigadores, más de la mitad de la población sufre problemas relacionados con el esmalte. Con el tratamiento nuevo, se aplicaría sobre los dientes una capa de proteínas que, al entrar en contacto con la saliva, formaría una fina cubierta de esmalte artificial mucho más dura y duradera que el barniz.
Una clave de esta técnica es que imita el proceso de biomineralización natural del esmalte. Los científicos parten de una matriz de proteínas que exponen a una disolución de fosfato de calcio, presente de forma natural en la saliva humana. Esta interacción hace que crezcan espontáneamente sobre las proteínas minerales de apatita o hidroxiapatita, incluso si la matriz se encuentre sobre una superficie irregular como un diente picado o desgastado. Igual que ocurre en la naturaleza, el esmalte sintético tiene una estructura cristalina organizada a diferentes escalas, desde el nivel nanométrico hasta estructuras visibles para el ojo humano. Esta organización jerárquica le confiere al mineral su característica rigidez, dureza y resistencia al ácido.
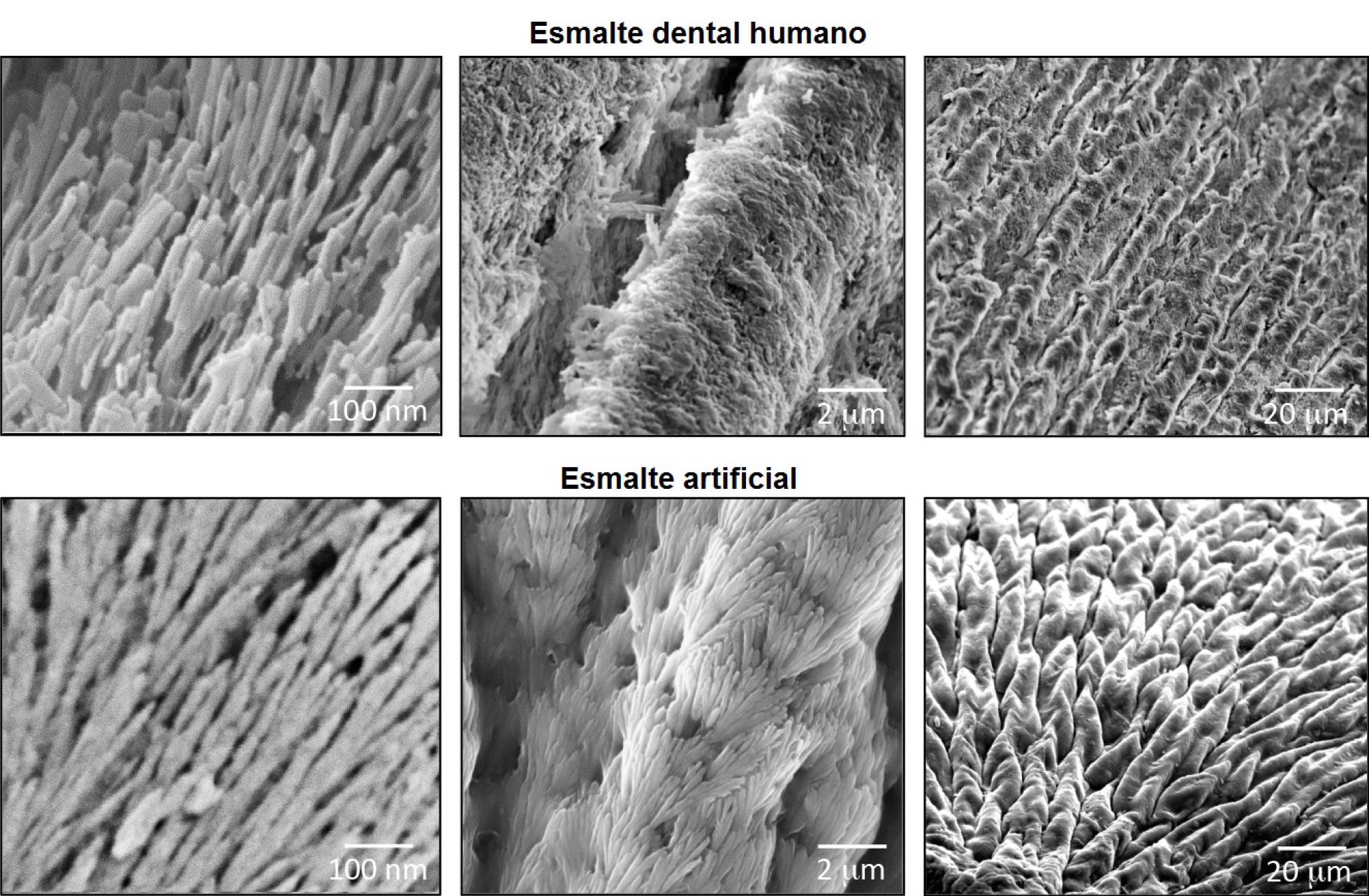
Comparación de las estructuras cristalinas del esmalte dental y de la estructura sintética, en diferentes escalas. / QUEEN MARY UNIVERSITY
El material sintético retiene un alto contenido orgánico (entre el 25% y 30% son proteínas), por lo que no es tan resistente como el esmalte natural. Sin embargo, esto mismo le confiere la capacidad de auto-regenerarse en caso de desgaste, señala Elsharkawy, algo que el esmalte dental no hace. En el estudio han colaborado investigadores de la Universidad de Valladolid, donde se fabrica la proteína recombinante que proporciona el andamiaje para los cristales. Ésta molécula incorpora elementos de la elastina (proteína estructural que confiere elasticidad a muchos tejidos) y de la estaterina (una proteína que se encuentra en la saliva y se adhiere al fosfato de calcio).
Estamos generando un material que se parece a hueso pero no necesita hueso para producirlo
“Parte de lo bonito de esto es que es súmamente fácil. Nosotros ponemos la proteína en disolución y luego la secamos. Pero hay un proceso que hacemos durante ese secado que permite controlar la rigidez de la proteína”, explica el bioingeniero de Queen Mary University Álvaro Mata, que también participó en la investigación. El éxito de la nueva técnica se debe en parte a los avances recientes en la comprensión de la fisiología dental: “Descubrimos que más importante que la composición química de la proteína es algo que ocurre con proteínas que tienen segmentos ordenados y desordenados”, agrega Mata. Los segmentos “desordenados” de las proteínas son tramos flexibles que les permiten cambiar su conformación para crear las estructuras jerárquicas, tan importantes en el esmalte dental. La presencia de estas regiones en la proteína sintética permite a los científicos guiar el crecimiento de los cristales y obtener las propiedades deseadas.
Además de las pruebas con dientes humanos, el equipo también está llevando a cabo pruebas en animales para desarrollar tratamientos óseos. “Estamos generando un material que se parece a hueso pero no necesita hueso para producirlo. Hay mucha necesidad para buscar materiales alternativos en ortopedia y en integración de implantes de hueso”, dice Mata. “También estamos pensando en opciones que no tienen nada que ver con la medicina. Estamos hablando con arquitectos para generar estructuras que puedan crecer de este material o, por ejemplo, pinturas protectoras”, concluye.



